原来的1/2倍和增大
原来的1/2倍和减小
减小和增大
不变和不变
第1题:
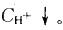
第2题:
在HAc-NaAc的混合液中,HAc和NaAc的浓度都为0.1mol/L,HAc的Ka=1.8×10-5。此缓冲溶液的pH值为()。
A4.74
B7.56
C8.86
D9.26
第3题:
A、加水
B、加NaAc
C、加0.1mol/LHCl溶液
第4题:
有下列溶液: ①0.01mol·L-1HAc溶液; ②0.01mol·L-1HAc与等体积等浓度的NaOH溶液混合; ③0.01mol·L-1HAc与等体积等浓度的HCl溶液混合; ④0.01mol·L-1HAc与等体积等浓度的NaAc溶液混合。 其pH值排列顺序正确的是()。
第5题:
将0.1mol/L的NaOH溶液与0.2mol/L的HAC溶液等体积混合,混合溶液具有缓冲作用。
第6题:
第7题:
下列各组溶液中,不能成为缓冲溶液的是()。
第8题:
在1mol/L的HAc溶液中,欲使H+浓度增大,可采取下列何种方法( )。
A.加水;
B.加NaAc;
C.加NaOH;
D.加0.1mol/L HCl溶液
第9题:
将0.1mol/L的HAc与0.1mol/L的NaAc混合溶液中加水稀释至原的体积的2倍,其H+浓度和pH值变化为()。
第10题:
以下各组溶液中,哪组不是缓冲溶液()。