第1题:
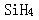
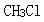
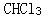
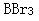
第2题:
甲烷,化学式CH4,分子是正四面体空间构型。
第3题:
下列化合物按沸点由高到低次序排列正确的是( )。
A、正丁烷>正己烷>丙烷>乙烷>甲烷
B、正己烷>正丁烷>丙烷>乙烷>甲烷
C、甲烷>乙烷>正己烷>丙烷>正丁烷
D、甲烷>乙烷>丙烷>正丁烷>正己烷
E、正丁烷>正己烷>甲烷>丙烷>乙烷
第4题:
甲烷分子不是以碳原子为中心的平面结构,而是以碳原子为中心的正四面体结构,其原因之一是甲烷的平面结构式解释不了下列事实()。
第5题:
根据价层电子对互斥理论,XeF4分子为正四面体结构
第6题:

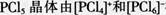 构成。且离子数目之比为1:1,A项正确,B项错误;PCI5在固态时由两种离子构成,属于离子晶体,两种离子之间存在离子键,C项错误;D项中该晶体中没有自由移动的离子或电子,不导电,D项错误。
构成。且离子数目之比为1:1,A项正确,B项错误;PCI5在固态时由两种离子构成,属于离子晶体,两种离子之间存在离子键,C项错误;D项中该晶体中没有自由移动的离子或电子,不导电,D项错误。第7题:
甲烷的分子构型是()。
第8题:
根据化合物相应的特征,由共价键构成,具有正四面体结构的是( )。
A.氟化氢;
B.冰;
C.甲烷;
D.氖
第9题:
Ni(CO)4、[Ni(CN)4]2-的空间结构分别是()
第10题:
下列说法正确的是()。