A1.526
B15.26
C152.6
D15.36
第1题:
下列混合溶液具有缓冲作用的是。
A、0.2mol·L-1的NH4Cl和0.2mol·L-1的NaOH溶液等体积混合
B、0.2mol·L-1的NH4Cl和0.1mol·L-1的NaOH溶液等体积混合
C、0.2mol·L-1的HAc和0.2mol·L-1的NaOH溶液等体积混合
D、0.2mol·L-1的NaAc和0.2mol·L-1的HCl溶液等体积混合
第2题:
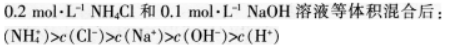
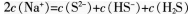
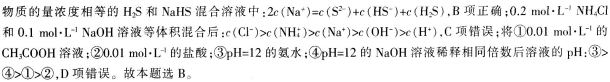
第3题:

第4题:
欲配制1000ml 0.1mol∕L的HCl溶液,应量取浓盐酸(12mol∕L)HCl()毫升?
第5题:
欲配制0.5000mol²L-1的盐酸溶液,现有0.4920mol²L-1的盐酸1000ml。问需要加入1.0210mol²L-1的盐酸()毫升。
第6题:

第7题:
欲配制1000mL,0.1mol/LHCl溶液,应取浓盐酸(12mol/L)多少毫升?()
第8题:
欲配制1000mL,0.1mol/LHCl溶液,应取浓盐酸(12mol/L)多少毫升?()
A.0.84mL
B.8.4mL
C.1.2mL
D.2.4mL
第9题:
配制6%的盐酸1000ml,若用8%的盐酸稀释,则还需要加水多少毫升?
第10题:
预配制9%的盐酸溶液100ml需要浓盐酸多少毫升;此盐酸溶液的M是多少?(假设市售浓盐酸的浓度为36%,密度1.2g/ml;10%的盐酸溶液的密度为0.3g/ml,以上浓度为质量百分比。)