第1题:
第2题:
下列物质碱性强弱规律如( )所示。
A.NaOH>Ca(OH)2>Ba(OH)2>Be(OH)2
B.NaOH>Be(OH)2>Ba(OH)2>Ca(OH)2
C.NaOH>Ba(OH)2>Be(OH)2>Ca(OH)2
D.NaOH>Ba(OH)2>Ca(OH)2>Be(OH)2
第3题:
A、[OH-]=[H+]+[Na+]
B、[OH]=[H+]-c
C、[OH-]=[H+]+c
D、[H+]=[OH-]-[Na+]
第4题:
在纯水中加入一些酸,则溶液中()
第5题:
第6题:
某溶液中[OH-]=1.0×10-5mol·L-1,则该溶液的pH为()
A、5
B、10
C、9
D、6
第7题:
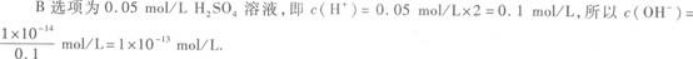
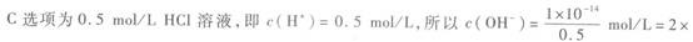
第8题:
下列溶液中微粒的物质的量浓度关系正确的是
A.室温下,向0.01 mol·L-1NH4HSO4溶液中滴加NaOH溶液至中性:c(Na+)>c(SO2-4)>c >c(OH-)=c(H+)
B.0.1 mol·L-1NaHCO3溶液:c(Na+)>c(OH-)>c(HCO3-)>c(H+)
C.Na2CO3溶液:c(OH-)-c(H+)=c(HCO3-)+2c(H2CO3)
D.25℃时,pH=4.75、浓度均为0.1 mol·L-1的CH3COOH、CH3COONa混合溶液:c(CH3COO-)+c(OH-)<c(CH3COOH)+C(H+)
第9题:
某溶液的pH值为2,说明该溶液().
第10题:
已知(Cr(OH)3)=6.3×10–31,反应Cr(OH)3+OH===[Cr(OH)4]-的平衡常数KΘ=0.40。 (1)计算Cr3+沉淀完全时溶液的pH值; (2)若将0.1mol·L–1Cr(OH)3刚好溶解在1.0LNaOH溶液中,则NaOH溶液的初浓度至少为多少? (3)计算[Cr(OH)4]-的标准稳定常数。