第1题:
反应的活化能是什么?它是怎样影响化学反应速率的?为什么有些反应的活化能很接近,反应速率却相差很大、但有些反应的活化能相差较大,反应速率却很接近?
答案:反应的活化能是指化学反应中,由反应物分子到达活化分子所需的最小能量。
化学反应速率与其活化能的大小密切相关。活化能越低,反应速率越快,因此降低活化能会有效地促进反应的进行。
从碰撞理论给出的公式k=Ae-Ea/RT 可以看出,Ea以指数关系影响速率常数k值,它的确是影响反应速率的重要因素,但A也影响k值。对不同的反应,A对k的影响很大,所以活化能不是决定反应速率的唯一因素。
第2题:
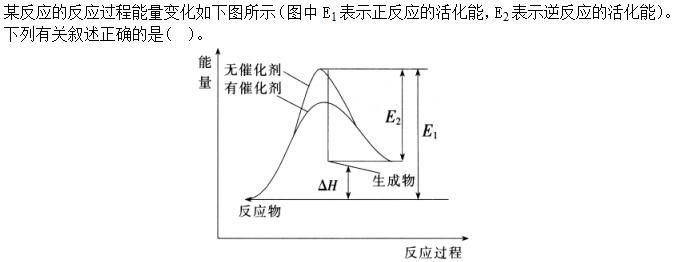
第3题:
根据Arrhenius方程,有关药物降解反应活化能的正确说法( )
A、活化能小的药物稳定性好
B、由lnC对t作图直线斜率即为活化能
C、由lgC对t作图直线斜率即为活化能
D、在一定温度范围内活化能为一定值
E、活化能具有能量单位
第4题:
反应A+B=AB的活化能是Ea,加入催化剂K后,反应历程发生变化,A+K=AK,活化能为E1,AK+B=AB+K,活化能为E2,(Ea>E2>E1)则加入催化剂后,反应的活化能为()
第5题:
活化能是使普通分子变为活化分子所需的最低能量,且活化能越低,反应速度越大。
第6题:
对两个活化能不同的反应,当温度同样从T1升至T2时,具有活化能高的反应,其反应速率增加的倍数比活化能低的反应增加的倍数。
A、小
B、大
C、一样
第7题:
简述活化能的概念。
第8题:
A、提高反应物的活性
B、提高反应的活化能
C、降低反应的活化能
D、没有作用
第9题:
关于反应的活化能,下列叙述正确的是()
第10题:
关于温度对高聚物表观黏流活化能的影响情况是()。