海水浸蚀过的镀锌板,形成的白锈,其主要成分为:()
第1题:
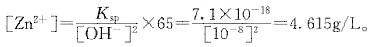
第2题:
镀锌零件发生锈蚀,生成的Zn0、Zn(OH)2锈蚀产物呈()。
第3题:
第4题:
既溶于过量氨水,又溶于过量NaOH溶液的是()
第5题:
对镀锌板钝化处理是为了防止镀锌板生"白锈"。
第6题:
投石灰以去除水中的Zn2+,生成Zn(OH)2沉淀,当pH=7或10时,问溶液中Zn2+的浓度各有多少?(mg/L)
第7题:
Fe(OH)2→Fe(OH)3为()锈。
第8题:
第9题:
镀锌板经过钝化、涂油处理之后,在任何情况下都不会产生白锈。
第10题:
Zn(OH)2受热会分解生成(),能溶于碱生成()