第1题:
碳是化学元素周期表中第二周期、第四主族元素,元素符号为( )。
第2题:
第3题:
元素在周期表中的位置,反映了元素的原子结构和元素的性质,下列说法正确的是
A.同一元素不可能既表现金属性,又表现非金属性
B.第三周期元素的最高正化合价等于它所处的主族序数
C.短周期元素形成离子后,最外层电子都达到8电子稳定结构
D.同一主族的元素的原子,最外层电子数相同,化学性质完全相同
第4题:
第5题:
第6题:


第7题:

第8题:
【题目描述】
第 2 题元素周期表是学习化学的重要工具。下面是元素周期表中1~18号元素原子核外电子排
布,我们对它进行研究:
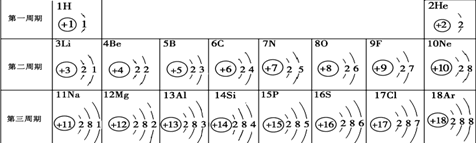
⑴ 第16号元素属于_______元素(填“金属”或“非金属”),它在化学反应中容易________(填“得”或“失”)电子;
⑵ 元素的化学性质与原子结构中的______________数关系密切;
⑶ 在同一族中,各元素的原子结构呈现的规律有________________ (任写一点);
⑷ 研究表明:第二周期从3~9号元素的原子电子层数相同,核电荷数逐渐增大,核对核外电子的引力逐渐增大,故原子半径逐渐减小。我分析第三周期从11~17号元素原子半径变化规律是 _________________________________。
参考答案分析】:
⑴ 非金属 ;得 ;
⑵ 最外层电子 ;
⑶ 电子层数递增或最外层电子数相等或从上到下核电荷数增大等(只要合理均可)⑷ 逐渐减小
第9题:
第10题: